Nom du produit:méthyléthylcétone
Format moléculaire :C4H8O
Numéro CAS :78-93-3
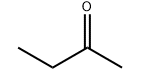
Structure moléculaire du produit:
Spécification:
| Article | Unité | Valeur |
| Pureté | % | 99,8 min |
| Couleur | APHA | 8max |
| Indice d'acidité (en tant qu'acide acétique) | % | 0,002max |
| humidité | % | 0,03 max |
| Apparence | - | Liquide incolore |
Propriétés chimiques:
La méthyléthylcétone est susceptible de diverses réactions en raison de son groupe carbonyle et de l'hydrogène actif adjacent à ce dernier. La condensation se produit lorsqu'elle est chauffée avec de l'acide chlorhydrique ou de l'hydroxyde de sodium pour produire de la 3,4-diméthyl-3-hexén-2-one ou de la 3-méthyl-3-heptén-5-one. Une exposition prolongée au soleil produit de l'éthane, de l'acide acétique et des produits de condensation. L'oxydation par l'acide nitrique produit du diacétyle. L'oxydation par des agents oxydants puissants comme l'acide chromique produit de l'acide acétique. La butanone est relativement stable à la chaleur et, à haute température, le clivage thermique produit de l'énone ou de la méthylénone. La condensation avec des aldéhydes aliphatiques ou aromatiques produit des cétones de haut poids moléculaire, des composés cycliques, des condensations cétoniques et des résines. Par exemple, la condensation avec du formaldéhyde en présence d'hydroxyde de sodium produit d'abord du 2-méthyl-1-butanol-3-one, suivi d'une déshydratation en méthacrylatone.
La résinisation se produit lors de l'exposition au soleil ou aux UV. La condensation avec le phénol produit du 2,2-bis(4-hydroxyphényl)butane. Réagit avec les esters aliphatiques en présence d'un catalyseur basique pour produire des β-dicétones. L'acylation avec l'anhydride acide en présence d'un catalyseur acide produit des β-dicétones. Réagit avec le cyanure d'hydrogène pour former de la cyanhydrine. Réagit avec l'ammoniac pour former des dérivés de la cétopipéridine. L'atome d'hydrogène α de la butanone est facilement substitué par des halogènes pour former diverses cétones halogénées, telles que la 3-chloro-2-butanone, par interaction avec le chlore. L'interaction avec la 2,4-dinitrophénylhydrazine produit de la 2,4-dinitrophénylhydrazone jaune.
Application:
La méthyléthylcétone (2-butanone, éthylméthylcétone, méthylacétone) est un solvant organique relativement peu toxique, utilisé dans de nombreuses applications. Elle est utilisée dans les produits industriels et commerciaux comme solvant pour les adhésifs, les peintures et les produits de nettoyage, ainsi que comme solvant de décirage. Composant naturel de certains aliments, la méthyléthylcétone peut être rejetée dans l'environnement par les volcans et les feux de forêt. Elle est utilisée dans la fabrication de poudres sans fumée et de résines synthétiques incolores, comme solvant et dans les revêtements de surface. Elle est également utilisée comme arôme dans les aliments.
La MEK est utilisée comme solvant dans divers systèmes de revêtement, notamment le vinyle, les adhésifs, la nitrocellulose et les revêtements acryliques. Elle est utilisée dans les décapants, les laques, les vernis, les peintures en aérosol, les produits d'étanchéité, les colles, les bandes magnétiques, les encres d'impression, les résines, les colophanes, les solutions de nettoyage et pour la polymérisation. On la retrouve dans d'autres produits de consommation, comme les ciments ménagers et de loisirs, et les produits de remplissage du bois. La MEK est utilisée dans le décirage des huiles lubrifiantes, le dégraissage des métaux, la production de cuirs synthétiques, de papier transparent et de feuilles d'aluminium, et comme intermédiaire chimique et catalyseur. C'est un solvant d'extraction dans la transformation des aliments et des ingrédients alimentaires. La MEK peut également être utilisée pour stériliser le matériel chirurgical et dentaire.
Outre sa fabrication, la MEK est présente dans l'environnement, notamment dans les gaz d'échappement des moteurs à réaction et à combustion interne, ainsi que dans les activités industrielles telles que la gazéification du charbon. On la retrouve en quantités importantes dans la fumée de tabac. La MEK est produite biologiquement et a été identifiée comme un produit du métabolisme microbien. On la retrouve également dans les plantes, les phéromones d'insectes et les tissus animaux. La MEK est probablement un produit mineur du métabolisme normal des mammifères. Stable dans des conditions normales, elle peut former des peroxydes en cas de stockage prolongé ; ceux-ci peuvent être explosifs.
Catégories de produits
-

Téléphone
-

E-mail
-

WhatsApp
-

Haut













